
Feb 07, 2024, 5:00 am UTC
Durée : 7 min
Created by
Des indices aux remèdes : pourquoi les biomarqueurs sont essentiels pour progresser dans la lutte contre les maladies neurodégénératives
L’année dernière, l’un des principaux sujets de la recherche sur les maladies neurodégénératives a été la découverte d’un biomarqueur de la maladie de Parkinson. Il a été annoncé en fanfare par la fondation de recherche sur la maladie de Parkinson de Michael J. Fox, qui soutient la recherche sur la découverte de biomarqueurs dans la maladie de Parkinson depuis environ deux décennies.
Les biomarqueurs sont des indicateurs puissants d’une maladie qui détiennent la clé d’une détection précoce, d’un diagnostic précis et de percées potentielles dans le traitement.
Pendant des décennies, le développement de traitements efficaces pour les maladies neurodégénératives telles que la maladie de Parkinson, la maladie d’Alzheimer et la maladie de Huntington, qui touchent des millions de personnes dans le monde et sont toujours incurables, a été difficile à mettre au point, en partie en raison de la complexité des processus biologiques à l’origine de ces maladies.
Aujourd’hui, la recherche de biomarqueurs pour les maladies neurodégénératives porte enfin ses fruits et catalyse des progrès urgents dans le domaine.
Cet article décomposera le concept de biomarqueurs, en mettant en lumière leurs diverses formes – des marqueurs génétiques aux protéines en passant par les indicateurs d’imagerie – et comment ils servent d’indices biologiques qui pourraient aider à percer les mystères des maladies neurodégénératives.
Cet article aborde les sujets suivants :
- Qu’est-ce qu’un biomarqueur ?
- Pourquoi sont-ils difficiles à découvrir ?
- Quels sont les différents types de biomarqueurs ?
- Quoi de neuf dans la découverte de biomarqueurs ?
- Pourquoi les biomarqueurs sont-ils nécessaires dans la recherche sur le cerveau ?
- Pourquoi les biomarqueurs spécifiques au sexe sont-ils nécessaires dans la recherche sur le cerveau ?
Qu’est-ce qu’un biomarqueur ?
Un biomarqueur – un mot-valise de « marqueur biologique » – est un indicateur mesurable de la biologie sous-jacente d’une maladie. Les biomarqueurs permettent d’identifier la présence d’un problème de santé, de surveiller la progression de la maladie et d’évaluer la façon dont le corps réagit au traitement. Ils fournissent également des informations précieuses sur les processus pathologiques sous-jacents et permettent aux chercheurs de suivre les changements liés à la maladie aux niveaux cellulaire et moléculaire.
L’un des biomarqueurs les plus utilisés en médecine est la pression artérielle, un indicateur du fonctionnement du système cardiovasculaire. Les résultats des tests d’imagerie des rayons X, des tomodensitogrammes et de l’imagerie par résonance magnétique (IRM) sont également utilisés comme biomarqueurs. Il en va de même pour les tests sanguins tels que l’hémoglobine A1c (HbA1c), qui signale qu’une personne a un taux de sucre dans le sang élevé et peut souffrir de prédiabète ou de diabète.
Cependant, pour les maladies neurodégénératives, les biomarqueurs ont été difficiles à trouver et sont donc rarement utilisés dans la recherche ou en clinique. Au lieu de cela, les gens sont diagnostiqués sur la base des seuls symptômes cliniques, qui apparaissent souvent tard dans le processus de la maladie une fois que des dommages au système nerveux se sont produits. À ce stade, il est souvent trop tard pour intervenir dans une maladie et faire une différence significative dans la vie d’un patient.
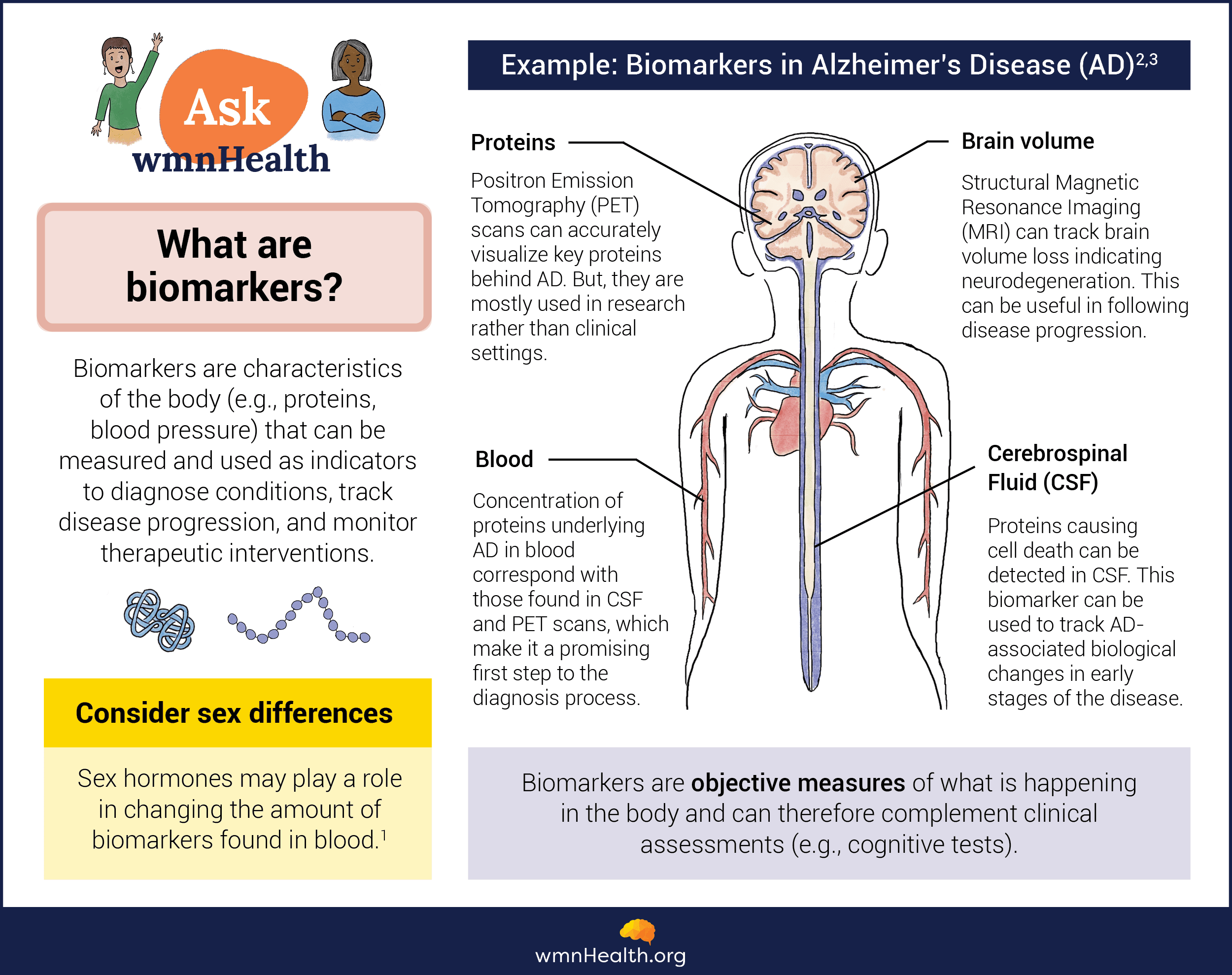 Infographie par Cat Lau. (Références ci-dessous.)
Infographie par Cat Lau. (Références ci-dessous.)Pourquoi est-il difficile de trouver des biomarqueurs pour les maladies neurodégénératives ?
Il est difficile de trouver des biomarqueurs fiables pour les maladies neurodégénératives pour plusieurs raisons. Premièrement, ces maladies sont complexes, impliquant de multiples composantes cellulaires et moléculaires, dont beaucoup sont encore à découvrir.
Deuxièmement, les maladies neurodégénératives sont très variables, ce qui signifie qu’elles peuvent se manifester différemment d’un individu à l’autre. Cette variabilité complique la découverte de biomarqueurs universels, qui reflètent fidèlement la maladie chez tout le monde.
Troisièmement, le cerveau est inaccessible par rapport à d’autres organes et tissus, ce qui rend difficile l’observation directe des changements biologiques associés aux maladies du cerveau. Bien qu’il soit possible d’obtenir une fenêtre sur le cerveau avec des échantillons d’imagerie et de liquide céphalo-rachidien, ces techniques nécessitent un équipement et une expertise spécialisés coûteux. Pour que les biomarqueurs soient utiles, ils doivent être accessibles, peu coûteux et faciles à appliquer.
Enfin, les maladies du cerveau comme la maladie d’Alzheimer ont souvent des caractéristiques pathologiques qui se chevauchent avec les processus normaux de vieillissement, ce qui rend difficile la recherche de biomarqueurs qui indiquent spécifiquement des changements spécifiques à la maladie plutôt que des altérations cérébrales liées à l’âge.
Cependant, malgré ces défis, les chercheurs continuent de faire des progrès dans la découverte de biomarqueurs pour les maladies neurodégénératives.
Quels sont les différents types de biomarqueurs ?
Divers types de biomarqueurs sont utilisés dans la recherche sur les maladies neurodégénératives, chacun fournissant des informations uniques sur le processus de la maladie. Ils peuvent être divisés en biomarqueurs « humides », qui se concentrent sur les indicateurs dans le sang, le sérum. la salive, le liquide céphalo-rachidien ou les tissus, ou les biomarqueurs « secs » comme les mutations génétiques, les mesures d’imagerie cérébrale et les indicateurs cliniques.
Biomarqueurs génétiques
Les biomarqueurs génétiques, tels que des mutations génétiques spécifiques, peuvent indiquer la susceptibilité d’un individu à développer une maladie neurodégénérative particulière. Par exemple, l’allèle ε4 APOE est fortement associé à un risque accru de développer la maladie d’Alzheimer.
Biomarqueurs biochimiques
Les biomarqueurs biochimiques, quant à eux, impliquent l’analyse de molécules spécifiques présentes dans les fluides corporels, tels que le sang ou le liquide céphalo-rachidien, un liquide qui baigne le cerveau et la moelle épinière et qui est riche en glucose, en protéines, en lipides et en électrolytes. Par exemple, la présence de niveaux anormaux de protéines bêta-amyloïde et tau dans le liquide céphalo-rachidien a été liée au développement de la maladie d’Alzheimer.
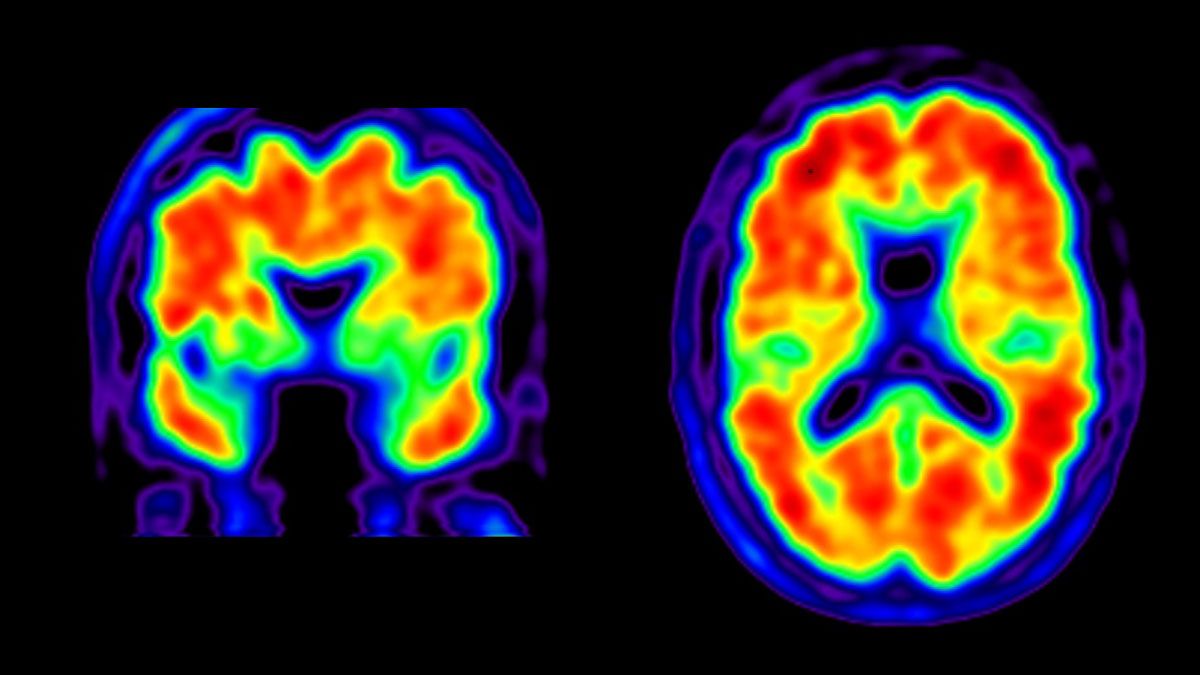 TEP amyloïde positive (Crédit : UCSF)
TEP amyloïde positive (Crédit : UCSF)Biomarqueurs d’imagerie
Les biomarqueurs d’imagerie s’appuient sur des techniques avancées d’imagerie cérébrale telles que l’IRM ou la tomographie par émission de positons (TEP) pour visualiser les changements moléculaires, structurels et fonctionnels dans le cerveau. Ces techniques peuvent fournir des informations précieuses sur la progression des maladies neurodégénératives, telles que la présence d’une atrophie cérébrale ou d’un dépôt anormal de protéines (photo).
Biomarqueurs cliniques
Les biomarqueurs cliniques, tels que les tests cognitifs, moteurs ou comportementaux, sont essentiels pour un diagnostic complet des maladies neurodégénératives et sont généralement associés à d’autres biomarqueurs. Par exemple, dans la maladie de Parkinson, un médecin peut combiner une échelle standard pour évaluer les mouvements d’une personne et un test d’alpha-synucléine anormale pour confirmer un diagnostic.
Biomarqueurs numériques
Les biomarqueurs numériques gagnent du terrain dans le domaine de la santé. Il s’agit de mesures objectives de la santé d’une personne dérivées de données recueillies et analysées à l’aide d’appareils numériques tels que des montres intelligentes ou des tablettes. Ils englobent un large éventail de mesures, notamment la variabilité de la fréquence cardiaque, les niveaux d’activité, les habitudes de sommeil, la température corporelle et la fonction cognitive.
Les biomarqueurs numériques promettent une surveillance continue et non invasive de l’état de santé d’une personne et une détection précoce. Cependant, le scepticisme persiste quant à leur adoption généralisée et à leur efficacité, en particulier dans des contextes réels.
Quoi de neuf dans la recherche sur la découverte de biomarqueurs pour la maladie de Parkinson et la maladie d’Alzheimer ?
Pour diagnostiquer la maladie d’Alzheimer, les médecins s’appuient encore fortement sur la documentation du déclin mental à l’aide des antécédents médicaux d’une personne, d’examens neurologiques et d’évaluations cognitives, psychologiques et fonctionnelles. Mais ils peuvent également prescrire des tests médicaux pour vérifier la présence de deux biomarqueurs : la bêta-amyloïde et la protéine tau. Ces deux protéines forment des dépôts cérébraux anormaux fortement liés à la maladie d’Alzheimer. La bêta-amyloïde et la protéine tau peuvent être détectées dans le liquide céphalo-rachidien à l’aide de tests biochimiques ou dans le cerveau à l’aide de technologies d’imagerie moléculaire telles que la TEP. Un ensemble différent d’outils d’imagerie est également couramment utilisé pour détecter les changements dans la structure et la fonction du cerveau dans la maladie d’Alzheimer.
Pourtant, les chercheurs s’efforcent de découvrir d’autres biomarqueurs de la maladie d’Alzheimer qui pourraient constituer un moyen simple, peu coûteux et non invasif de diagnostiquer la maladie. Par exemple, des biomarqueurs dans le sang, l’urine et la salive, ainsi que dans l’œil pourraient être utilisés pour détecter la maladie à un stade précoce.
Le biomarqueur de la maladie de Parkinson annoncé l’année dernière utilise l’alpha-synucléine anormale, une protéine qui se replie mal et forme des amas dans les cellules des personnes atteintes de la maladie de Parkinson, comme indicateur de la maladie. Les chercheurs ont mis au point un outil, le test d’amplification des graines d’alpha-synucléine (ɑSyn-SAA), pour détecter la protéine mal repliée dans le liquide céphalo-rachidien des personnes diagnostiquées avec la maladie de Parkinson. L’outil amplifie de minuscules quantités d’alpha-synucléine mal repliée dans des échantillons de personnes atteintes de la maladie de Parkinson afin que la protéine puisse être facilement détectée en laboratoire. Aujourd’hui, pour la première fois, la maladie de Parkinson peut être diagnostiquée biologiquement chez une personne vivante. Les outils peuvent également détecter une anomalie de l’alpha-synucléine chez les personnes à risque de contracter la maladie, mais qui n’ont pas encore développé de symptômes ou n’ont pas encore été diagnostiquées.
Les biomarqueurs de la maladie de Parkinson ne se limitent pas à l’alpha-synucléine. Les chercheurs étudient également la possibilité d’utiliser une protéine appelée neurofilament light (Nfl), une mesure sensible des dommages neuronaux et une enzyme appelée DOPA décarboxylase comme biomarqueurs de la maladie de Parkinson. La perte de l’odorat et les changements de sommeil sont également à l’étude. De plus, les chercheurs mettent au point des tests d’alpha-synucléine qui peuvent détecter les amas de protéines mal repliés dans la peau ou le sang, ce qui rend l’échantillonnage beaucoup plus facile et rentable.
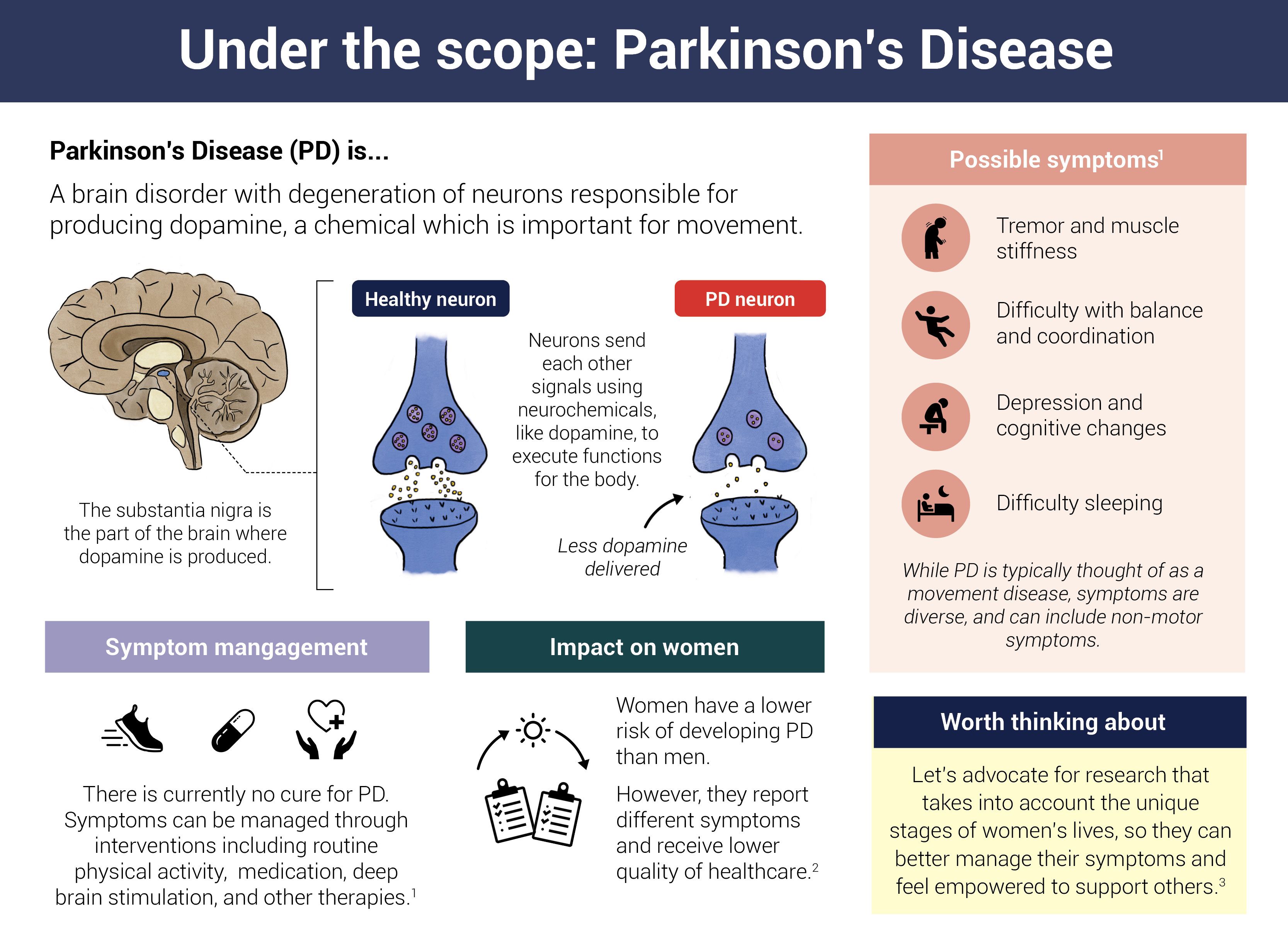 Infographie par Cat Lau. (Références ci-dessous.)
Infographie par Cat Lau. (Références ci-dessous.)Comment les biomarqueurs des maladies neurodégénératives peuvent-ils contribuer à transformer la recherche et les soins ?
Les principales utilisations des biomarqueurs sont la détection précoce, le diagnostic et le suivi de la progression de la maladie.
Détection précoce
En identifiant des biomarqueurs corrélés à l’apparition de la maladie, les chercheurs peuvent mettre au point des tests de dépistage qui permettent aux médecins d’agir avant que des dommages irréversibles ne surviennent.
Une étude publiée dans The New England Journal of Medicine a démontré l’utilité des biomarqueurs pour prédire l’apparition de la maladie d’Alzheimer. Les chercheurs ont découvert que la combinaison d’un biomarqueur génétique (allèle APOE ε4) et d’un biomarqueur biochimique (niveaux de protéines bêta-amyloïdes) leur permettait de prédire avec précision l’apparition de la maladie jusqu’à 20 ans avant l’apparition des symptômes.
De plus, les biomarqueurs peuvent aider à différencier les maladies neurodégénératives qui peuvent présenter des symptômes cliniques similaires. Cette distinction est cruciale car elle permet des approches de traitement ciblées et adaptées à la pathologie spécifique de la maladie.
Diagnostic précis
Diagnostiquer les maladies neurodégénératives avec précision et efficacité reste un défi de taille. Les biomarqueurs offrent une solution prometteuse en fournissant des mesures objectives qui complètent les évaluations cliniques.
Par exemple, les critères du Groupe de travail international (IWG) pour le diagnostic de la maladie d’Alzheimer incluent désormais des preuves de biomarqueurs d’anomalies de la bêta-amyloïde et de la protéine tau en plus des symptômes cliniques. En intégrant ces biomarqueurs biochimiques de la maladie d’Alzheimer, les médecins peuvent l’identifier à ses débuts, avant même qu’un déclin cognitif significatif n’apparaisse.
Le mois dernier, des experts ont publié un système similaire pour diagnostiquer et stadifier la maladie de Parkinson en utilisant une combinaison de biomarqueurs, notamment une alpha-synucléine anormale, une dégénérescence de la dopamine dans le cerveau et des symptômes cliniques tels que des troubles moteurs et non moteurs. Selon le système proposé, un individu dont les neurones ont une alpha-synucléine mal repliée, mais qui ne présente aucun symptôme de la maladie de Parkinson, est au stade zéro. Au fur et à mesure que la maladie se développe, une personne passera par les stades trois à six à mesure que sa déficience fonctionnelle augmentera.
Surveillance de l’évolution de la maladie
La capacité de surveiller la progression de la maladie est cruciale pour comprendre l’évolution naturelle des maladies neurodégénératives et évaluer si les traitements potentiels ont un impact.
En surveillant régulièrement les biomarqueurs, les chercheurs et les cliniciens peuvent suivre l’évolution de la gravité de la maladie, identifier les personnes les plus susceptibles de bénéficier de traitements spécifiques et évaluer la façon dont les patients réagissent aux traitements. Ce type de données peut également aider à développer et à évaluer de nouvelles thérapies dans le cadre d’essais cliniques.
Une étude récente publiée dans The Lancet Neurology a démontré le potentiel des biomarqueurs dans le suivi de la progression de la maladie de Parkinson. Les chercheurs ont utilisé une combinaison d’imagerie et de biomarqueurs biochimiques pour suivre la propagation de l’alpha-synucléine anormale. Cette compréhension détaillée de la progression de la maladie peut contribuer à la mise au point de thérapies ciblées visant à arrêter ou à retarder la progression de la maladie.
Pourquoi les biomarqueurs spécifiques au sexe sont-ils nécessaires pour les maladies neurodégénératives ?
Les maladies neurodégénératives présentent souvent des différences spécifiques au sexe en termes de prévalence de la maladie, de symptômes et de progression. Par conséquent, il est essentiel de comprendre ces différences et de développer des biomarqueurs spécifiques au sexe pour améliorer le diagnostic et les résultats du traitement chez les femmes et les hommes. En identifiant des biomarqueurs spécifiques au sexe, les chercheurs peuvent également mieux comprendre les mécanismes sous-jacents à l’origine de ces différences.
Par exemple, des études ont montré que les femmes sont plus susceptibles de développer la maladie d’Alzheimer que les hommes, mais on ne sait pas exactement pourquoi. Il existe également des différences dans l’accumulation de bêta-amyloïde et de tau dans le cerveau des femmes et des hommes. Encore une fois, les chercheurs ne comprennent pas entièrement pourquoi.
L’une des hypothèses concerne le système immunitaire. Un système immunitaire dysfonctionnel est en train de devenir un moteur de la maladie d’Alzheimer. Dans le même temps, il est également largement reconnu que les femmes sont touchées de manière disproportionnée par les troubles immunitaires par rapport aux hommes. Ces différences immunitaires pourraient-elles expliquer pourquoi la maladie d’Alzheimer est plus fréquente chez les femmes, pourquoi la pathologie est différente chez les femmes et pourquoi les femmes ont tendance à décliner plus rapidement que les hommes après le diagnostic ? Les chercheurs tentent de le savoir en identifiant des biomarqueurs spécifiques au sexe de la maladie, qui pourraient inclure des mesures du système immunitaire.
La découverte de biomarqueurs permet de mieux comprendre les maladies neurodégénératives et de faire progresser leur diagnostic, leur traitement et leur surveillance. Cependant, il reste encore des défis à relever pour libérer le plein potentiel des biomarqueurs afin d’améliorer la vie des personnes touchées par ces maladies, y compris l’optimisation des biomarqueurs pour une utilisation dans la recherche et en clinique, la mise en œuvre pratique et la nécessité de biomarqueurs spécifiques au sexe.
Références infographiques
Qu’est-ce qu’un biomarqueur ?
- Sex differences in biomarkers impact clinical testing, Women's Health Research Institute (accessed January 23, 2024)
- Dubois, B., von Arnim, C.A.F., Burnie, N. et al. Biomarkers in Alzheimer’s disease: role in early and differential diagnosis and recognition of atypical variants. Alz Res Therapy 15, 175 (2023).
- Klyucherev, T.O., Olszewski, P., Shalimova, A.A. et al. Advances in the development of new biomarkers for Alzheimer’s disease. Transl Neurodegener 11, 25 (2022).
Mettre en lumière : Maladie de Parkinson
- Parkinson's Disease, National Institutes of Health (Accessed June 9, 2023)
- Women and PD, Parkinsons.org (Accessed June 9, 2023)
- Subramanian, I., et al. Unmet Needs of Women Living with Parkinson's Disease: Gaps and Controversies. Movement Disorders, Vol. 37, No. 3, 2022


