Feb 20, 2024, 5:00 am UTC
7 min
Created by
¿La enfermedad de Alzheimer es genética y hay que hacerse la prueba?
Para las personas que tienen familiares -abuelos, padres o incluso hermanos- con enfermedad de Alzheimer (EA), esta afección puede parecer inevitable. Sin embargo, según los expertos, no es fácil responder a la pregunta: "¿Tendré yo el mismo destino?
Cada uno de los seis millones de estadounidenses que padecen EA, de los que aproximadamente dos tercios son mujeres, se encuentra en un viaje diferente. Los síntomas varían mucho, la progresión es impredecible y las causas no se comprenden bien. En medio de esta incertidumbre, los antecedentes familiares pueden parecer el único indicador fiable -y crucial- del riesgo de desarrollar la enfermedad.
Ahora es más fácil que nunca saber lo que se ha heredado o no de los padres gracias a nuevas pruebas que revelan marcadores genéticos relacionados con la enfermedad. Algunas de estas pruebas pueden hacerse incluso en casa. Pero, como ocurre con cualquier avance tecnológico, hay que tener cuidado. He aquí la primicia.
Este artículo trata sobre:
¿Qué genes se han identificado como factores de riesgo de la enfermedad de Alzheimer?
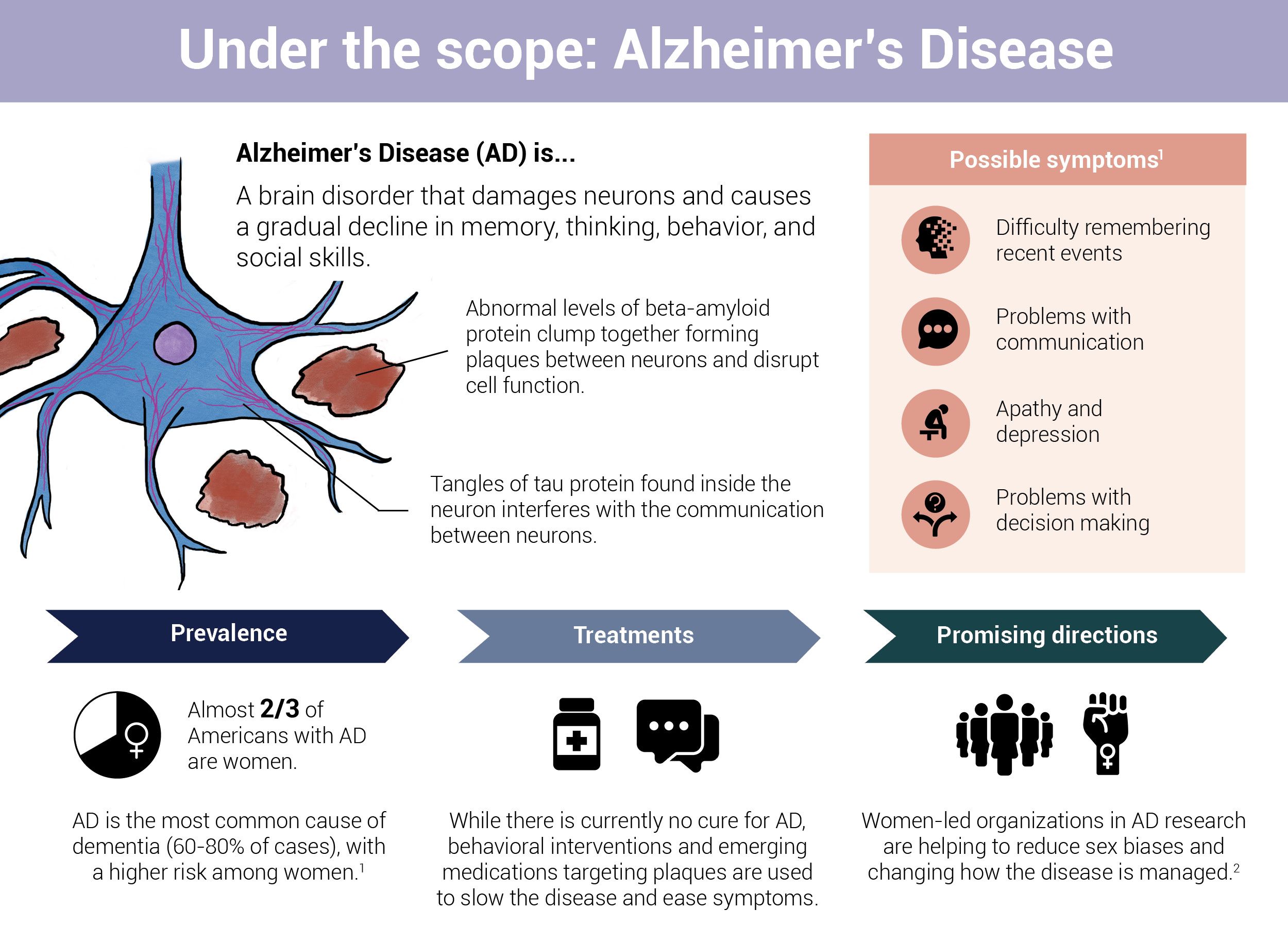
Las placas y los ovillos neurofibrilares, que contienen proteínas beta amiloide y tau, respectivamente, son características distintivas de la enfermedad de Alzheimer. Cuando estas proteínas naturales se alteran, empiezan a agruparse y enredarse dentro y alrededor de las neuronas. Esto altera la función celular, dificulta la comunicación entre neuronas y desencadena una respuesta inmunitaria inflamatoria que acaba degenerando y matando las células cerebrales.
Hay muchas razones -algunas mejor comprendidas que otras- que contribuyen al mal funcionamiento de estas proteínas. Una de ellas son los problemas en el "manual de instrucciones" para la construcción de proteínas. Estas instrucciones son transportadas por pequeños segmentos de ADN, también conocidos como genes, que se transmiten de una generación a la siguiente. Cada gen tiene dos copias o alelos. Juntos, el par de alelos -uno heredado de cada progenitor- influye en todo, desde el color de los ojos y la piel hasta el funcionamiento de las células.
Infografía de Cat Lau. (Referencias más abajo.)
Sin embargo, el proceso de transmisión de estas instrucciones de generación en generación no es infalible. En ocasiones, un alelo puede sufrir cambios químicos espontáneos que alteren el código genético transmitido de padres a hijos.
Los investigadores han identificado más de 60 genes que podrían estar implicados en la EA. Estos genes se dividen en dos grandes categorías: Genes deterministas y genes de riesgo.
Genes deterministas
Los genes deterministas están asociados a formas raras de EA de aparición temprana. Las mutaciones en estos genes conducen directamente al desarrollo de la EA con un alto grado de certeza.
Afortunadamente, la probabilidad de que una persona desarrolle Alzheimer debido a la presencia de un único gen determinista es rara. De hecho, menos del 5 por ciento de todos los casos de EA se consideran Enfermedad de Alzheimer Familiar (EAF). Este tipo de Alzheimer se caracteriza por la herencia de una mutación en uno de los tres genes que regulan la producción de beta amiloide: Proteína precursora de amiloide (APP), Presenilina 1 (PSEN1) y Presenilina 2 (PSEN2).
- APP (Proteína precursora de amiloide): Piense en la APP como una proteína más grande que se rompe en fragmentos más pequeños conocidos como beta amiloide. Cuando se producen mutaciones en el gen APP, este proceso de fragmentación se descontrola, dando lugar a una producción excesiva de beta amiloide. Este exceso de fragmentos de beta amiloide se aglutina en las células cerebrales, alterando procesos celulares críticos.
- PSEN1 (Presenilina 1) y PSEN2 (Presenilina 2): Los genes de la presenilina intervienen en la regulación de cómo -y cuánta- proteína APP se fragmenta en beta amiloide. Las mutaciones en estos dos genes pueden cambiar la composición y los niveles de beta amiloide en el cerebro.
Genes de riesgo
Los genes de riesgo (o susceptibilidad) aumentan la probabilidad de desarrollar EA, pero no garantizan la enfermedad. Estos genes están relacionados con un tipo común de EA, conocida como enfermedad de Alzheimer de inicio tardío o LOAD (por sus siglas en inglés), que suele comenzar en torno a los 65 años y en la que influyen diversos factores genéticos, ambientales y de estilo de vida. La LOAD es esporádica, lo que significa que no es hereditaria.
A continuación se enumeran algunos genes de riesgo asociados a la EA, pero se han descubierto docenas más:
- APOE (Apolipoproteína E): El gen APOE tiene tres formas o alelos comunes denominados e2, e3 y e4. Los estudios demuestran que el alelo APOE e4 está asociado a una mayor acumulación de beta amiloide en el cerebro. Las razones exactas de esta acumulación siguen sin estar claras, pero los investigadores plantean la hipótesis de que está relacionada con el papel de APOE e4 en el metabolismo de los lípidos (grasas) y el colesterol en el organismo.
- Las personas que heredan una copia del APOE e4 tienen un mayor riesgo a lo largo de su vida de desarrollar Alzheimer. Las personas con dos copias de este alelo tienen un riesgo aún mayor de desarrollar la enfermedad a lo largo de su vida. (Esta asociación es especialmente cierta en las personas de ascendencia blanca no hispana). Además, las mujeres con un alelo APOE e4 tienen un riesgo significativamente mayor de desarrollar EA que los hombres.
- CLU (Clusterina): El gen CLU ayuda a producir una proteína llamada clusterina, que es crucial para degradar y eliminar la beta amiloide en el cerebro. Sin embargo, ciertas variaciones de este gen dan lugar a la producción de un tipo menos eficiente de clusterina. Esta ineficacia puede provocar una acumulación de beta amiloide.
- SORL1 (Receptor 1 relacionado con la Sortilina): SORL1 actúa como un controlador del tráfico en el cerebro, determinando lo que ocurre con la proteína APP. Normalmente, SORL1 aleja la APP de la vía que produce beta amiloide. Sin embargo, ciertas variaciones de SORL1 no hacen este trabajo con la misma eficacia, lo que conduce a una sobreproducción de beta amiloide.
Es importante señalar que gran parte de lo que se sabe sobre el riesgo genético de Alzheimer se basa en investigaciones con participantes blancos de ascendencia europea. Está mucho menos claro cómo influye la genética en la susceptibilidad a la EA en otras poblaciones.
Alelo APOE e4
- Se calcula que entre el 20 y el 30 por ciento de los estadounidenses tienen una o dos copias del alelo APOE e4.
- Aproximadamente el 2% de la población estadounidense tiene dos copias de APOE e4.
Fuente: Asociación de Alzheimer
¿Influye el sexo de una persona en el riesgo genético de padecer Alzheimer?
La respuesta corta es sí. Además, cada vez hay más pruebas de que las diferencias de sexo en el riesgo genético van más allá del APOE e4, que aumenta la probabilidad de que una mujer con una o dos copias del alelo desarrolle Alzheimer. Investigadores de la Universidad de California en San Diego desarrollaron puntuaciones de riesgo de Alzheimer para hombres y mujeres combinando los efectos de docenas de cambios genéticos, la mayoría asociados por sí mismos a un riesgo reducido de padecer la enfermedad. Descubrieron que las puntuaciones de riesgo eran mejores para predecir la edad de aparición y los cambios cerebrales relacionados con la enfermedad cuando se emparejaban con el sexo, es decir, las puntuaciones de riesgo masculinas se emparejaban con las masculinas y las femeninas con las femeninas. Los resultados sugieren que el sexo de una persona influye en su riesgo genético de padecer Alzheimer, aunque aún no está claro qué cambios genéticos son los responsables.
¿Deberías someterte a una prueba genética para detectar el Alzheimer, sopesando sus ventajas e inconvenientes?
Las pruebas genéticas para detectar el Alzheimer no son rutinarias, aunque cada vez son más frecuentes. De hecho, no existen pruebas fiables que puedan predecir la forma más común de Alzheimer: la EA de aparición tardía. Sin embargo, existen pruebas para los genes raros que causan directamente el Alzheimer y el APOE e4, y un médico puede recomendarlas en circunstancias específicas.
Ekaterina Rogaeva, del Centro Tanz de Investigación en Enfermedades Neurodegenerativas de la Universidad de Toronto, ha dedicado los últimos 30 años a la investigación genética del Alzheimer y ha contribuido al desarrollo de pruebas que permiten buscar marcadores asociados a esta enfermedad. Sin embargo, hasta hace poco, estas pruebas no han servido a los médicos para determinar el riesgo de Alzheimer.
Por un lado, no ha habido ningún tratamiento eficaz en el mercado que pueda ralentizar la progresión de la enfermedad. "En ese caso, el conocimiento sólo puede causar un intenso estrés y hacer que la gente tenga la nerviosa esperanza de escapar a esta devastadora afección", afirma Rogaeva.
Y no hay que olvidar que las mutaciones genéticas no son las únicas culpables de esta enfermedad: factores ambientales y psicosociales como la dieta, el ejercicio, el compromiso social e incluso la educación influyen mucho en la reserva cognitiva, es decir, en la capacidad del cerebro para hacer frente a los cambios que, de otro modo, provocarían la EA.
Los factores de riesgo de la enfermedad de Alzheimer son:
Antecedentes familiares: Tener un familiar cercano (padre, hermano o hermana) con enfermedad de Alzheimer aumenta el riesgo de desarrollarla.
Genética: Diversas mutaciones genéticas pueden aumentar el riesgo de padecer Alzheimer, aunque sólo unos pocos cambios genéticos causan directamente la enfermedad.
Edad: El mayor factor de riesgo de la enfermedad de Alzheimer es la edad.
Lesiones cerebrales traumáticas: Las personas con lesiones cerebrales previas pueden tener un mayor riesgo de desarrollar la enfermedad de Alzheimer.
Salud cardiaca: Los daños en el corazón o los vasos sanguíneos causados por cardiopatías, diabetes, accidentes cerebrovasculares, hipertensión arterial y colesterol alto pueden aumentar el riesgo de desarrollar la enfermedad de Alzheimer.
Estilo de vida: Factores modificables como la dieta, el sueño, el ejercicio, el tabaquismo, el consumo de alcohol y las relaciones sociales pueden influir en el riesgo de padecer Alzheimer.
Pero las cosas han cambiado con la aprobación de Leqembi. Este fármaco puede eliminar la acumulación de beta amiloide y ralentizar el ritmo de deterioro cognitivo en personas con Alzheimer, pero con el riesgo de inflamación y hemorragias cerebrales. Ahora aumentan las pruebas genéticas para detectar la enfermedad: Un análisis muestra que, en los meses previos a la aprobación de Leqembi en EE.UU., el número de personas mayores de 55 años que se sometieron a pruebas genéticas de APOE e4 aumentó un 125%.
En algunas situaciones, las pruebas pueden ayudar a orientar las decisiones terapéuticas. Por ejemplo, las personas con el alelo APOE e4 tienen un mayor riesgo de sufrir efectos secundarios graves con los fármacos antiamiloides. La advertencia es que una puntuación de riesgo genético alta no siempre garantiza que una persona desarrolle la enfermedad. De hecho, los hallazgos de un estudio de 2019 publicado en la revista JAMA sugieren que un estilo de vida saludable puede ayudar a compensar el riesgo genético de demencia. Un grupo de investigadores del Reino Unido siguió a 200.000 personas con distintos niveles de riesgo genético de demencia durante ocho años, evaluando sus hábitos de vida. Descubrieron que entre las personas con un alto riesgo genético, sólo el 1 por ciento de las que mantenían un estilo de vida saludable desarrollaron demencia. En cambio, casi el doble de las personas con malos hábitos de vida desarrollaron demencia.
"La mayor parte de las investigaciones se han realizado en varones caucásicos, por lo que no comprendemos tan bien como deberíamos las diferencias genéticas basadas en el sexo y la raza en la enfermedad de Alzheimer", afirma Rogaeva.
La Alzheimer's Association de Estados Unidos y la Alzheimer's Society de Canadá desaconsejan las pruebas genéticas para detectar el Alzheimer en personas sanas. Las pruebas genéticas caseras, que no requieren la aprobación de un médico, son especialmente preocupantes porque puede que no se disponga de asesoramiento para ayudar a las personas a interpretar los resultados de las pruebas.
En definitiva, las pruebas genéticas, en su forma actual, no son adecuadas, ni siquiera eficaces, para todo el mundo. Confiar en ellas para diagnosticar el Alzheimer es como montar un rompecabezas con sólo una parte de las piezas: útil, pero lejos de estar completo.
Referencias de la Infografía
- 2023 Alzheimer's Facts and Figures: Special Report, Alzheimer's Association (Consultado el 20 de Enero de 2023)
- Castro-Aldrete L, Moser MV, Putignano G, Ferretti MT, Schumacher Dimech A and Santuccione Chadha A (2023) Sex and gender considerations in Alzheimer’s disease: The Women’s Brain Project contribution. Front. Aging Neurosci. 15:1105620.